4. Что не является ошибкой?
Некоторые особенности построения фазовых диаграмм иногда причисляются к ошибкам без должного на то основания.
Первая группа проблем, связанных с псевдоошибками - это изображение стехиометрических соединений без области гомогенности, а также отсутствие областей твердых растворов на основе компонентов.
Строго говоря, из термодинамических и молекулярно-кинетических соображений следует, что при температуре, отличной от абсолютного нуля, всегда имеет место какая-то, хотя бы малая, взаимная растворимость любых веществ, а также диссоциация соединений. Действительно, химический потенциал растворенного вещества бесконечно убывает при уменьшении его концентрации, что свидетельствует о нарастании трудностей очистки с уменьшением концентрации примеси и невозможности полного удаления примесей. Соответствующее уравнение выглядит следующим образом:
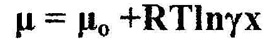
где мю - химический потенциал, x - концентрация примеси, гамма - коэффициент активности, R - газовая постоянная. Этот вопрос подробно разобран у Ван-дер-Ваальса [9] , см. также [10, 49] .
Из обязательного наличия твердых растворов на основе всех соединений и их частичной диссоциации при нагревании вытекает ряд следствий [7]:
1) несовпадение температуры полиморфного перехода в двойной системе с температурой полиморфного перехода у компонента;
2) различие температур полиморфного перехода у соединения справа и слева от области или ординаты его состава;
3) невозможность существования идеальной вырожденной эвтектики;
4) невозможность существования сингулярных максимумов;
Необходимо помнить, однако, что все явления диссоциации и взаимной растворимости могут быть очень незначительно выражены и выявляются только при специальных прецизионных исследованиях. Например, если мы изучаем бинарную систему, беря составы через 5 мол %, мы не заметим области твердых растворов протяженностью порядка 1%; если частота точек 1%, мы не обнаружим области твердых растворов порядка 0,1% и т.д. Для обнаружения твердых растворов ~ 10-2 - 10-3 % требуются специальные методы исследования (например, измерения давления пара или электропроводности). Такие области гомогенности никак не могут быть показаны при обычном масштабе изображения полной диаграммы состояния.
Если строго следовать точке зрения, что стехиометрических соединений не существует, то некорректно вообще рассматривать системы типа хлорид магния - хлорид алюминия и строить их фазовые диаграммы: ввиду частичной диссоциации соединений необходимо изучать тройную систему магний-алюминий-хлор и строить ее фазовую диаграмму. Этот пример показывает, что определенная степень идеализации, т.е. рассмотрение на каком-то этапе исследований недиссоциирующих соединений, эвтектических диаграмм состояния без образования твердых растворов и т.п., не только возможно, но и необходимо.
Для любого промежуточного соединения равновесная область гомогенности пренебрежимо мала вблизи абсолютного нуля температуры. При повышении температуры она расширяется, и, начиная с некоторого момента, становится заметной. Таким образом, для каждого соединения существует некоторая эффективная температура, зависящая от метода и целей исследования, ниже которой соединение можно рассматривать как стехиометрическое, а выше – как нестехиометрическое. Для некоторых соединений эта температура будет ниже температуры плавления или разложения.
Таким образом, если в результате исследования твердые растворы не выявлены, и с точностью эксперимента не удается, например, зафиксировать сдвиг температуры фазового перехода соединения при добавлении компонента, то нет необходимости рисовать не обнаруженные области гомогенности пунктиром; при реальной ширине областей твердых растворов на несколько порядков меньше изображенного пунктирные области будут грубой ошибкой. В таких случаях лучше указать, что твердые растворы не обнаружены с такой-то точностью.
При любом масштабе изображения существует температура, ниже которой область твердого раствора или область гомогенности соединения сливается в линию.
Высказывалась точка зрения, что области гомогенности фаз на диаграмме состояния необходимо указывать независимо от реальной протяженности этих твердых растворов и масштаба изображения (см. например, [50]). С этим мнением трудно согласиться, т.к. утрирование одной из особенностей диаграммы превращает ее из документа в карикатуру.
В некоторых случаях, однако, изображение на фазовой диаграмме области гомогенности фазы обязательно, даже если границы ее не выявлены в ходе эксперимента. Это относится к случаям, когда отличаются друг от друга температуры полиморфных переходов, зафиксированные справа и слева от ординаты соединения (в концентрационных областях, содержащих избыточное и недостаточное содержание одного из компонентов по отношению к стехиометрии).
Пример такой фазовой диаграммы представлен на рис. 29а. Линии E1-F1 и G2-H2 очевидно, относятся к фазовому переходу с упорядочением при охлаждении высокотемпературной модификации фазы идеализированного состава К2UBr6 (структурный тип К2PtCl6, кубич. сингония), имеющей область гомогенности. Вариант корректной диаграммы состояния представлен на рис. 29b. Характерно, что термический анализ может не фиксировать никаких промежуточных температур "полиморфного превращения” и трехфазные горизонтали могут подходить справа и слева практически вплотную к идеализированному составу соединения и даже перекрываться. Этo обстоятельство, в частности, ставило в тупик авторов работы [52], зафиксировавших такую ситуацию для соединения К3InCl6 (рис. 29c).
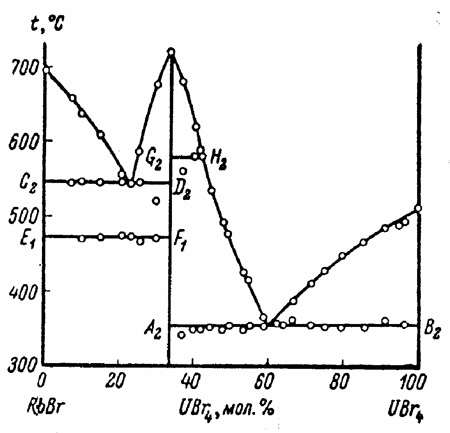
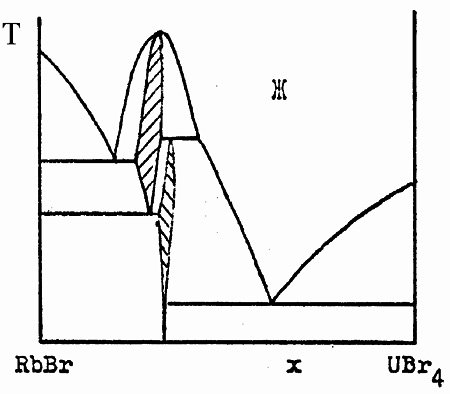
Рис. 29. Т-х фазовая диаграмма системы RbBr – UBr4 по данным [22] (а) и предполагаемая схема фазовых равновесий в этой системе (b). Заштрихованные поля – области гомогенности фаз.
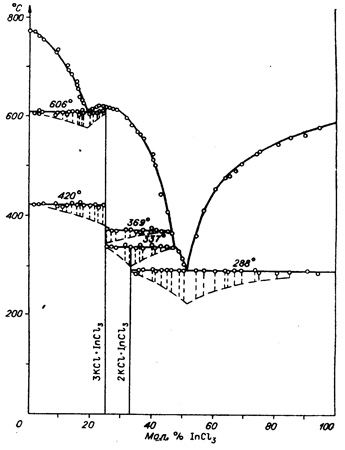
Рис. 29c. Т-х фазовая диаграмма системы KCl – InCl3 по данным [51]. Область гомогенности на основе высокотемпературной модификации K3InCl6 не отмечена.
Вторая группа особенностей, oбычно трактуемая как ошибки при построении фазовых диаграмм - это четырехфазные горизонтали на диаграммах состояния бинарных систем. Такие случаи иногда наблюдались экспериментально, см. рис. 31 и 11. На этих рисунках изображены четырехфазные равновесия: Ж+ K4Na2Ti3O9 + KNaTiO3 + Na2TiO3 при 800 °С, рис. 31, и RbF + Rb3ErF6 + Rb2ErF5 + RbEr2F7 при 60 °С, рис. 11.
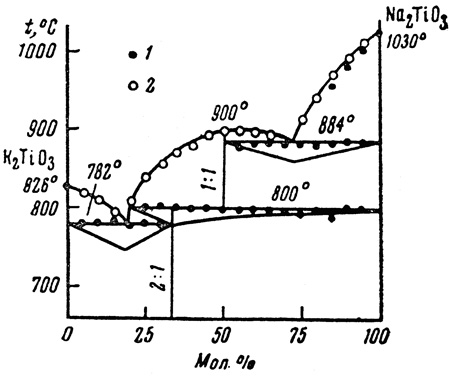
Рис. 30. Т-х фазовая диаграмма системы K2TiO3 - Na2TiO3 по данным [52].
Рассмотрим вопрос о четырехфазных равновесиях в двойных системах подробно. Если в правиле фаз (уравнение (2)) считать переменной только температуру (ф = I), то в двойной системе (К = 2) максимальное число фаз, находящихся в равновесии, равно трем. Случаи, изображенные на рис. 30 и 11 как будто невозможны и содержат ошибку. Однако, ситуация может изменится, если мы рассмотрим возможность изменения давления. Тогда ф = 2 и максимальное число равновесных фаз равно четырем. Нонвариантное равновесие четырех фаз на Р - Т - x диаграмме существует при некоторых фиксированных значениях температуры и давления. Если мы изучаем систему именно при соответствующем давлении, мы и получим на ней равновесие четырех фаз.
Последовательность Т - х сечений Р - Т - х диаграммы двойной системы, содержащую переходное сечение типа изображенного на рис. 20, представлена на рис. 31. Классификация такого рода переходных диаграмм состояния бинарных систем дана в [13].
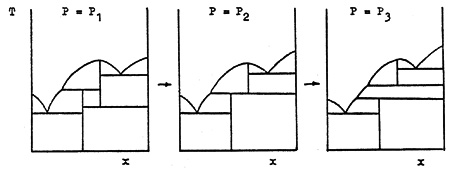
Рис. 31. Т-х сечения фазовой диаграммы двойной системы, отвечающие инверсии температурной устойчивости промежуточных фаз.
Экспериментально изучая систему при каком-то давлении, например, атмосферном, невозможно ожидать, что мы попадем точно на нонвариантное равновесие. В руководстве Райнза [1] получение четырехфазных горизонталей на Т - х диаграмме бинарной системы названо "невероятным”. Однако, мы вполне можем оказаться весьма близко к давлению, отвечающему четырехфазному равновесию, так что обычные экспериментальные методики не позволяют нам отличить реальную диаграмму состояния с двумя близкими по температуре трехфазными равновесиями от переходного случая с четырьмя равновесными фазами.
Необходимо учитывать, что эти рассуждения справедливы для конденсированных фаз, когда газовая фаза не участвует в равновесии, т.е. если мы работаем в открытых тиглях в инертной (по отношению к изучаемым веществам) атмосфере. Именно такому случаю отвечает диаграмма на рис. 30.
Если же мы изучаем систему в запаянных ампулах (именно такая методика и использована при изучении системы RbF – ErF3, рис.11), то одной из равновесных фаз является пар. В таком случае равновесия трех конденсированных фаз (в частности, обычные эвтектики) отвечают уже четырехфазным равновесиям с участием пара. В этих случаях равновесия четырех конденсированных фаз возможны только при учете, кроме температуры и давления, других внешних факторов, например электромагнитного поля. Для диэлектриков это маловероятно, и изображение четырехфазной горизонтали на рис.11, по-видимому, является ошибкой.
Таким образом, диаграммы типа, изображенного на рис. 30, нельзя сразу трактовать как ошибочные. Но эти случаи заслуживают самого тщательного изучения с использованием комплекса методов физико-химического анализа.
Однако, появление более чем одной четырехфазной горизонтали на Т-х фазовой диаграмме бинарной системы уже очевидно невозможно. В соответствии с этим, изобарическое сечение фазовой диаграммы, представленной на рис. 32, которое содержит около 20 четырехфазных равновесий, необходимо трактовать как содержащее рекордное количество ошибок.
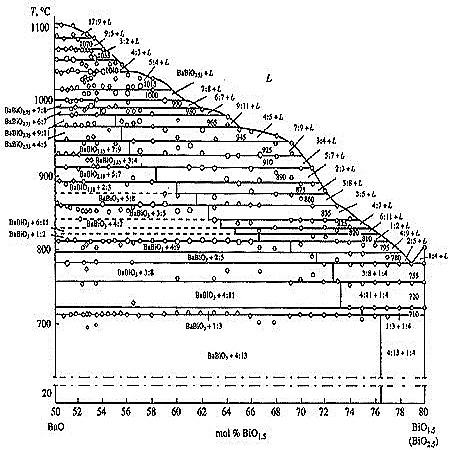
Рис. 32. Фрагмент Т-x фазовой диаграммы политермического разреза системы Ba-Bi-O при рО2 = 0.21атм по [53].
